Il colore delle Aurore: da cosa dipende?

In poche parole il colore delle Aurore dipende dalla lunghezza d'onda della luce emessa che è determinata degli elementi che sono presenti in atmosfera, dai lori stati elettronici, dalla loro altezza e dall'energia delle particelle che li colpiscono.
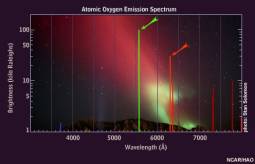
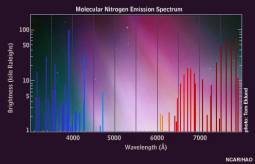
In atmosfera gli elementi predominanti sono l'Ossigeno e l'Azoto. Sappiamo che l'Ossigeno se eccitato ritorna nel suo stato naturale emettendo principalmente due colori: il Verde (lunghezza d'onda di 557.7 nm) ed il Rosso (630,0 nm), mentre l'Azoto emette color Blu, Viola e Rosso.
Analizzando l'atmosfera Ossigeno è l'elemento più abbondante ad altitudini superiori a 300 km, ove le pressioni e le concentrazioni sono però assai basse. A queste altitudini quando una molecola di ossigeno viene eccitata impiega meno di un secondo ad emettere un fotone verde mentre può impiegare anche 2 minuti ad emetterne uno rosso. Data la scarsa concentrazione le collisioni tra atomi e molecole sono in genere molto basse pertanto l'ossigeno ha tutto il tempo di emettere il fotone di colore rosso, dando origine a rare aurore rosse.
Man mano che scendiamo nell'atmosfera la densità delle molecole aumenta e quindi le collisioni con gli atomi vengono via via più frequenti. A poco a poco le emissioni di fotoni rossi si attenuano sino a divenire quasi nulle.
Ad altitudini tra i 180 km (112 miglia) a 300 km (186 miglia), i brillamenti di colore giallo-verdi, i più frequenti nelle aurore, sono prodotte dalle combinazioni dei fotoni verdi emessi dall'ossigeno ed i fotoni blu e rosso emessi dall'azoto. Ricordiamo infatti che a queste altitudini, l'ossigeno perde la sua capacità di emettere fotoni rossi.
Sotto i 120 km (74 miglia) le emissioni di luce blu da parte dell'azoto ionizzato e rosso da parte dell'azoto eccitato creano il bordo rosso porpora intenso delle aurore. A queste altitudini inferiori gli atomi di ossigeno non hanno la possibilità di emettere né verde né luce rossa.